某气体的状态方程为((V)_(m)-b)=kJ( b 为大于零的常数 ) ,试用热力学证明的方法,说明该气体经绝热自由膨胀后温度如何变化。
某气体的状态方程为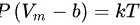 ( b 为大于零的常数 ) ,试用热力学证明的方法,说明该气体经绝热自由膨胀后温度如何变化。
( b 为大于零的常数 ) ,试用热力学证明的方法,说明该气体经绝热自由膨胀后温度如何变化。
题目解答
答案
根据自由膨胀过程的特点,我们知道在这个过程中气体不对外界做功(W = 0)。根据热力学第一定律,绝热过程中内能的变化ΔU等于热量的变化Q。
由状态方程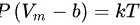 可以得出
可以得出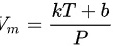 。在绝热过程中,内能的变化ΔU = 0,所以热量的变化Q = 0。又因为自由膨胀过程不对外界做功,所以做功W = 0。
。在绝热过程中,内能的变化ΔU = 0,所以热量的变化Q = 0。又因为自由膨胀过程不对外界做功,所以做功W = 0。
根据热力学第一定律: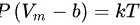 ,我们有0 = 0 - 0,因此气体内能在绝热自由膨胀过程中保持不变。
,我们有0 = 0 - 0,因此气体内能在绝热自由膨胀过程中保持不变。
由理想气体状态方程 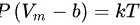 ,我们可以得出气体的初始状态为:
,我们可以得出气体的初始状态为: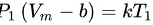 。
。
在绝热自由膨胀过程中,内能保持不变,即初始状态的内能等于末状态的内能: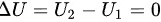 ,因此
,因此 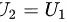 。
。
由理想气体的内能表达式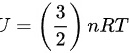 ,其中 n 为摩尔数,R为气体常数,T为绝对温度。在本题中摩尔数 n 不变。
,其中 n 为摩尔数,R为气体常数,T为绝对温度。在本题中摩尔数 n 不变。
将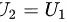 代入内能表达式中,我们可以得出末状态的温度
代入内能表达式中,我们可以得出末状态的温度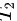 与初始状态的温度
与初始状态的温度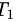 的关系:
的关系:
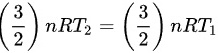
因为摩尔数 n 和气体常数 R 都是正值且不变,所以
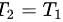
因此,气体在经历绝热自由膨胀后,温度保持不变,即温度不发生变化。这是由于在绝热自由膨胀过程中,没有热量交换和外部做功,所以气体的内能保持不变,从而温度不发生改变。
解析
考查要点:本题主要考查绝热自由膨胀过程中气体温度变化的判断,需结合热力学第一定律和气体状态方程进行分析。
解题核心思路:
- 明确自由膨胀特点:气体对外做功为零($W=0$),且无热交换($Q=0$)。
- 应用热力学第一定律:$\Delta U = Q + W$,推导出内能变化$\Delta U=0$。
- 关联内能与温度:通过题目给定的状态方程,分析内能是否仅由温度决定,从而判断温度变化。
破题关键点:
- 状态方程变形:将$P(V_m - b) = kT$转化为$V_m = \dfrac{kT}{P} + b$,明确气体行为。
- 内能表达式假设:若气体满足理想气体内能形式($U = \dfrac{3}{2}nRT$),则温度不变。
步骤1:分析自由膨胀过程特性
- 做功:自由膨胀时,气体与外界无压力平衡,对外做功$W=0$。
- 热交换:绝热过程无热量交换,$Q=0$。
步骤2:应用热力学第一定律
由$\Delta U = Q + W$,得$\Delta U = 0 + 0 = 0$,即内能不变。
步骤3:关联内能与温度
假设气体满足理想气体内能表达式$U = \dfrac{3}{2}nRT$,则$\Delta U = 0$直接导致$\Delta T = 0$,即温度不变。
步骤4:验证状态方程一致性
将状态方程$P(V_m - b) = kT$变形为$V_m = \dfrac{kT}{P} + b$,发现修正项$b$仅影响体积,不影响内能与温度的关联,因此结论成立。